약물관련 악골괴사증
1. 약물 관련 악골 괴사증(Medication-Related Osteonecrosis of the Jaw, MRONJ)의 진단 기준 1
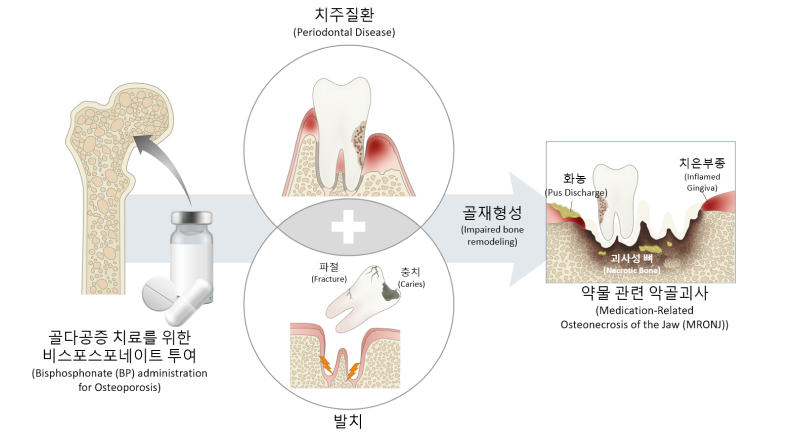
약물 관련 악골괴사는 1) 현재 또는 이전에 골흡수억제제 혹은 혈관형성 억제제 투여를 받고, 2) 8주 이상 악안면 부위의 구내 혹은 구외로 생긴 누공을 통해 뼈를 관찰 및 탐침할 수 있거나 뼈가 노출된 경우, 3) 악골에 방사선 치료의 병력 또는 명확한 전이성 질환의 병력이 없음에도 뼈가 노출된 경우로 3가지 모두를 만족할 때를 약물 관련 악골괴사(MRONJ)라 정의한다.
2. 약물 관련 악골 괴사증의 병태생리(Pathophysiology of MRONJ)
-
골흡수 및 골재형성의 억제
신체 골격에서 파골세포의 분화와 기능은 골치유와 재형성에 중요한 역할을 한다. MRONJ를 유발하는 약물인 비스포스포네이트(bisphosphonates) 및 데노수맙(denosumab)과 같은 골흡수 억제제는 파골세포의 분화와 기능을 억제하고 세포자멸사(apoptosis)를 촉진시키고 골재흡수를 감소시켜 골재형성을 억제한다. 1
악골괴사(Osteonecrosis of the Jaw, ONJ)는 대부분 위턱뼈(maxillary bone)와 아래턱뼈(mandibular bone)의 치조골에 주로 발생한다.1 악골에서 골재형성이 발생함에 따라 상대적으로 높은 농도의 약물이 축적되는 것이 주요인으로 추정되고 있다. 비스포스포네이트 뿐 아니라 데노수맙과 같은 다른 종류의 골흡수 억제제에서도 골재형성이 억제되어 ONJ 발생에 영향을 미치는 것으로 알려져 있다.1
-
감염과 염증 (Infection & Inflammation)
염증과 감염은 오랫동안 악골괴사를 유발시킬 수 있는 중요한 인자로 생각되었다. 여러 임상 연구를 통해 치과관련 질환이나 세균 감염이 악골괴사 발병과 연관 있다고 보고된다.1,2 초기에 발표된 증례들은 대부분 발치와 관련이 있었는데, 이들은 치주질환이나 치근단 질환에 이환되어 있는 상태였다.1 염증과 감염이 존재하는 상태에서 골흡수억제제의 투여가 ONJ를 유발하게 된다는 유의미한 결과가 몇몇의 동물모델 연구를 통해 발표되었다. 1,3
ONJ에 이환된 골편의 생검을 통해 세균(특히,방선균류(Actinomycetes)의 집락)이 확인되었다.1 또한, 이어진 연구에서 곰팡이류(fungi), 바이러스(virus)와 함께 세균(bacteria)의 존재가 확인되었다. 이는 표면 괴사조직 제거술, 항생제 함유 구강세정제의 이용 및 전신적인 항생제 처방과 같은 치료방법의 필요성을 뒷받침한다.1,4,5
-
혈관 형성 억제 (Angiogenesis inhibition)
혈행 공급 중단이나 무혈관성 괴사*(avascular necrosis*)로 인해 ONJ가 발병된다는 것을 바탕으로 혈관형성 억제가 ONJ 병인의 주된 가설이 된다.1 졸레드론산(zoledronic acid)으로 악성종양 환자를 치료하여 혈관내피성장인자(Vascular Endothelial Growth Factor, VEGF)가 감소된 연구33와 혈관 형성 억제제 (Tyrosine kinase inhibitors 또는 VEGF등)를 투여한 환자에서 ONJ 발생 사례가 증가되었다는 연구1 등에 의거하여 졸레드론산이 혈관 신생률 감소에 영향을 미치는 것을 확인하였다.1 (*혈액 공급이 원활하지 못하여 뼈가 썩는 병)
-
연조직 독성 (Soft tissue toxicity)
비스포스포네이트는 기본적으로 파골세포의 분화 작용을 억제하나, 연조직에 대한 독성도 있는 것으로 보고되었다.1 체외 실험으로 비스포스포네이트에 노출된 여러 종류(자궁경부, 전립선, 경구의 상피세포)의 세포에서 세포자멸사가 증가되거나 증식이 감소되는 경향을 보였다.1,7 대조적으로 데노수맙은 연조직 독성에 대한 보고는 없다.
-
악골에서만 특이적으로 생기는 원인에 대한 가설1
악골은 상피세포를 뚫고 나오는 치아를 지지하고 있어, 구강내의 감염원이 직접적으로 노출된 악골에 영향을 줄 수 있다. 구강은 약1011–1012개의 박테리아가 800종 이상 존재하여 세균이 번식하기 매우 적합한 환경을 조성하므로 이들이 상존하여 직접 감염 및 2차 감염의 원인이 될 수 있다.8 악골은 인체의 다른 골과 달리 매우 얇은 점막과 골막으로 최소 보호되어 감염 및 외상에 취약하다.8 또한 발치 등의 침습적 치과 치료 후에는 골이 쉽게 구강내로 노출된다.8 치아 우식, 치수염, 치근단병소, 치주질환 등 높은 유병률의 감염성 치과 질환을 통해 염증이 악골로 전파될 수 있다.
악골은 다른 장골에 비해 혈행 공급이 활발하고, 골재형성률이 높다는 특징을 가지고 있다.9 이는 확률적으로 비스포스포네이트 등의 약물이 다른 골에 비해 고농도로 악골에 침착 될 수 있음을 시사한다.1
References
- 1. Ruggiero, Salvatore L., et al. "American Association of Oral and Maxillofacial Surgeons position paper on medication-related osteonecrosis of the jaw—2014 update." Journal of oral and maxillofacial surgery 72.10 (2014): 1938-1956.
- 2. Dayisoylu, E. H., et al. "The effects of adjunctive parathyroid hormone injection on bisphosphonate-related osteonecrosis of the jaws: an animal study." International journal of oral and maxillofacial surgery 42.11 (2013): 1475-1480.
- 3. Mawardi, Hani, et al. "Sinus tracts—an early sign of bisphosphonate-associated osteonecrosis of the jaws?" Journal of oral and maxillofacial surgery 67.3 (2009): 593-601.
- 4. Hansen, Torsten, et al. "Osteonecrosis of the jaws in patients treated with bisphosphonates–histomorphologic analysis in comparison with infected osteoradionecrosis." Journal of oral pathology & medicine 35.3 (2006): 155-160.
- 5. Kos, Marcin, et al. "Pamidronate enhances bacterial adhesion to bone hydroxyapatite. Another puzzle in the pathology of bisphosphonate-related osteonecrosis of the jaw?" Journal of Oral and Maxillofacial Surgery 71.6 (2013): 1010-1016.
- 6. Bezzi, Manuela, et al. "Zoledronate sensitizes endothelial cells to tumor necrosis factor-induced programmed cell death: evidence for the suppression of sustained activation of focal adhesion kinase and protein kinase B/Akt." Journal of Biological Chemistry 278.44 (2003): 43603-43614.
- 7. Giraudo, Enrico, Masahiro Inoue, and Douglas Hanahan. "An amino-bisphosphonate targets MMP-9–expressing macrophages and angiogenesis to impair cervical carcinogenesis." The Journal of clinical investigation 114.5 (2004): 623-633
- 8. Yoneda, Toshiyuki, et al. "Bisphosphonate-related osteonecrosis of the jaw: position paper from the allied task force committee of Japanese society for bone and mineral research, Japan osteoporosis society, Japanese society of periodontology, Japanese society for oral and maxillofacial radiology, and Japanese society of oral and maxillofacial surgeons." Journal of bone and mineral metabolism 28.4 (2010): 365-383.
- 9. McCauley, L. K., and Xin Li. "Distinguishing features of the oral cavity and its predisposition to osteonecrosis." JOURNAL OF MUSCULOSKELETAL AND NEURONAL INTERACTIONS 7.4 (2007): 356.
1. 전신적 위험 요인(Systemic factors)
- 악성종양
- 고령
- 항암화학요법
- 여성
- 방사선치료
- 스테로이드 장기 투여
- 당뇨
- 흡연
- 장기간 약물에 노출된 경우
- 골다공증
- 혈관형성억제제 투여
- 정주투여(경구투여 대비)
치료 목적에 관계없이 비스포스포네이트 등의 골흡수 억제제를 사용하거나, 관련 약제에 노출된 기간이 긴 경우(exposed duration) ONJ 위험 요인으로 본다. 주사제재가 경구제재에 비해 높은 위험요인이라는 다수의 보고가 있으나, 사용 약제의 적응증을 고려한다면 유의하지 못한 경우가 많아 이에 대해서는 아직까지 논란이 되고 있다.
장기간 코르티코스테로이드(Corticosteroids)를 사용 시 위험도가 증가한다.1 코르티코스테로이드는 항염증 효과가 있는 모든 스테로이드 약물을 통틀어 일컫는 말로 면역질환, 천식과 호흡기 질환, 관절 질환에서 장기적으로 사용된다.
당뇨 환자는 건전하지 못한 골질, 미세혈관 허혈, 내피세포 장애, 골재형성의 감소 및 골세포와 골형성세포의 사멸 등으로 인해 ONJ의 위험요인으로 추정된다. 2,3
또한 고령일수록 여성일수록 ONJ 발생 빈도가 높다. 이는 폐경 후 골다공증 또는 유방암 등 여성암과 관련된 약물을 복용하는 빈도가 높아지는 것과 관련 있다.1,2,4,5 다만, 남성과 비교하여 여성이 ONJ 위험 요인이 된다는 증거는 아직까지 많지 않다.
그 외 위험 요인으로는 악성종양, 방사선치료, 항암화학요법, 혈관형성 억제제 투여, 유전학적 위험 요인 등이 제시되고 있다.1 또한 명확한 근거는 없으나, 여러 역학 연구에서 빈혈 및 인종을 위험요인으로 보고 있다. 이전에는 백인(Caucasian)종에서 호발한다고 보고되었지만, 현재는 아시아인종(Asian)의 약물유전학적 취약성 또한 주목받고 있다. 유전적 위험 요인으로 CYP2C815-16, RBMS31, COL1A1, RANK, MMP2, OPG, OPN1등이 제시되었다.
2. 국소적 위험 요인(Local factors)
- 발치
- 치과 임플란트
- 의치(틀니) 사용
- 치조골 수술
- 해부학적 요소
- 치주염 및 치근단염
발치를 시행한 치조골과 치아치조수술(dentoalveolar surgery)은 명확하게 알려진 ONJ 위험요인이다. ONJ 발병의 52~62%가 치아 발치 후 발생한다고 알려져 있으며, 발치의 위험도는 16.5~33배로 보고된다.
치과 임플란트 식립술 및 관련 자가골, 이종골, 합성골 이식술은 이미 알려진 위험요인이다. 다만, 수술적 요인 이외에도 이미 성공적으로 식립이 되어 기능을 하고 있는 임플란트가 ONJ를 유발할 수 있다는 여러 보고가 있다. 의치(틀니) 사용, 특히 의치의 지지부위가 점막인 경우 점막에 자극이 되면서 ON유발과 관련이 있다. 염증성 치과 질환인 치주염 또는 치근단염 또한 ONJ 발생을 증가시킨다.
해부학적으로 위턱뼈(22.5%)보다는 아래턱뼈(73%)에서 빈발하지만, 양측(4.5%)에서 나타나는 경우도 있다.
References
- 1. Ruggiero, Salvatore L., et al. "American Association of Oral and Maxillofacial Surgeons position paper on medication-related osteonecrosis of the jaw—2014 update." Journal of oral and maxillofacial surgery 72.10 (2014): 1938-1956.
- 2. Barasch, A., et al. "Risk factors for osteonecrosis of the jaws: a case-control study from the CONDOR dental PBRN." Journal of dental research 90.4 (2011): 439-444.
- 3. Peer, A., and M. Khamaisi. "Diabetes as a risk factor for medication-related osteonecrosis of the jaw." Journal of dental research 94.2 (2015): 252-260.
- 4. Lee, Jeong Keun, et al. "Bisphosphonates-related osteonecrosis of the jaw in Korea: a preliminary report." Journal of the Korean Association of Oral and Maxillofacial Surgeons 39.1 (2013): 9.
- 5. Brown, J. J., L. Ramalingam, and M. R. Zacharin. "Bisphosphonate‐associated osteonecrosis of the jaw: does it occur in children?." Clinical endocrinology 68.6 (2008): 863-867.
- 6. Ruggiero, Salvatore L., et al. "American Association of Oral and Maxillofacial Surgeons position paper on medication-related osteonecrosis of the jaw—2014 update." Journal of oral and maxillofacial surgery 72.10 (2014): 1938-1956.
- 7. Zervas, Kostas, et al. "Incidence, risk factors and management of osteonecrosis of the jaw in patients with multiple myeloma: a single‐centre experience in 303 patients." British journal of haematology 134.6 (2006): 620-623.
- 8. Cafro, Anna Maria, et al. "Osteonecrosis of the jaw in patients with multiple myeloma treated with bisphosphonates: definition and management of the risk related to zoledronic acid." Clinical Lymphoma and Myeloma 8.2 (2008): 111-116.
- 9. Wessel, John H., et al. "Zoledronate, smoking, and obesity are strong risk factors for osteonecrosis of the jaw: a case-control study." Journal of Oral and Maxillofacial Surgery 66.4 (2008): 625-631.
- 10. Bujanda, D. Aguiar, et al. "Assessment of renal toxicity and osteonecrosis of the jaws in patients receiving zoledronic acid for bone metastasis." Annals of oncology 18.3 (2007): 556-560.
- 11. Lesclous, Philippe, et al. "Bisphosphonate-associated osteonecrosis of the jaw: a key role of inflammation?." Bone 45.5 (2009): 843-852.
- 12. Jadu, F., et al. "A retrospective study assessing the incidence, risk factors and comorbidities of pamidronate-related necrosis of the jaws in multiple myeloma patients." Annals of Oncology 18.12 (2007): 2015-2019.
- 13. Thumbigere-Math, Vivek, et al. "A retrospective study evaluating frequency and risk factors of osteonecrosis of the jaw in 576 cancer patients receiving intravenous bisphosphonates." American journal of clinical oncology 35.4 (2012): 386-392.
- 14. Vescovi, Paolo, et al. "Surgery-triggered and non surgery-triggered Bisphosphonate-related Osteonecrosis of the Jaws (BRONJ): A retrospective analysis of 567 cases in an Italian multicenter study." Oral Oncology 47.3 (2011): 191-194.
- 15. English, Bevin C., et al. "A SNP in CYP2C8 is not associated with the development of bisphosphonate-related osteonecrosis of the jaw in men with castrate-resistant prostate cancer." Therapeutics and clinical risk management 6 (2010): 579.
- 16. Sarasquete, Maria E., et al. "Bisphosphonate-related osteonecrosis of the jaw is associated with polymorphisms of the cytochrome P450 CYP2C8 in multiple myeloma: a genome-wide single nucleotide polymorphism analysis." Blood 112.7 (2008): 2709-2712.
- 17. Kwon, Tae‐Geon, et al. "Osteonecrosis associated with dental implants in patients undergoing bisphosphonate treatment." Clinical Oral Implants Research 25.5 (2014): 632-640.
- 18. Jacobsen, Christine, et al. "Osteopathology induced by bisphosphonates and dental implants: clinical observations." Clinical oral investigations 17.1 (2013): 167-175.
- 19. Lazarovici, Towy Sorel, et al. "Bisphosphonate-related osteonecrosis of the jaw associated with dental implants." Journal of Oral and Maxillofacial Surgery 68.4 (2010): 790-796.
1. 약물 관련 악골괴사증(MRONJ)의 유발 약물1
-
골흡수 억제제(antiresorptives)
- 비스포스포네이트(bisphosphonates) 계열 약물: pamidronate, alendronate, risedronate, ibandronate, zoledronate
-
RANKL 인간단일클론 항체* (Receptor activator of nuclear factor kappa-B ligand): denosumab
*한가지 항원에 대해 한 종류의 항체만 생성하는 항체를 말하며, 사람의 암세포나 특정 단백질을 동물에 주사하여 이들의 면역반응으로 단클론항체를 생산한다. 특정 물질을 추적하는 진단시험이나 면역반응을 이용하는 치료에 사용되며, 이들 계열 약물들은 영어 약인 ‘mAb’을 사용하여 ‘-맙’의 형태로 불린다.
- 스클러로스틴 표적 단일클론 항체(Sclerostin-binding monoclonal antibody): romosozumab2
-
골다공증의 치료를 위해 사용되는 약물은 아니지만 MRONJ을 유발할 수 있다고 알려져 있는 약물(Antiangiogenic or Targets of the Vascula Endothelial Growth Factor (VEGF) Pathway)
- 인산화효소 억제제(Tyrosine kinase inhibitor): sunitinib, sorafenib
- 인간 단일클론항체(Humanized monoclonal antibody): bevacizumab
- Mammalian target of rapamycin pathway: sirolimus
2. 약물 관련 악골 괴사증의 병기1
명백한 괴사골이 보이지 않는 정주 또는 경구 항흡수제제 또는 혈관형성억제제로 치료받은 무증상 환자를 MRONJ의 위험군(patient at risk)으로 보고 있다. 악골괴사는 증상 및 임상적 소견에 따라 분류되어 0~3까지의 단계로 나타낼 수 있다.
-
Stage 0 (None-exposed bone variant)
괴사골의 임상적인 증거가 없으나, 다음과 같이 비특이적인 증상 또는 임상 및 영상 소견을 보인다. 치성을 원인으로 하여 설명되지 않는 치통, 턱관절부위까지 퍼질 수 있는 아래턱뼈의 둔통(dull, aching bone pain), 신경 감각기능의 변형의 증상을 보인다.
임상적 소견으로는 만성 치주질환으로 설명되지 않는 치아 상실, 치아우식으로 인한 치수 괴사와 연관되지 않는 치근단 또는 치주조직의 누공 등이 있다. 만성 치주질환의 원인이 아닌 치조골의 상실 또는 흡수, 골소주 패턴(trabecular pattern)의 변화(: 치밀한 교직골(dense woven bone)과 재형성되지 않은 골(unremodeled bone)이 지속적으로 존재), 치조골과기저골을 포함한 골경화(osteosclerosis) 부위, 비후하거나 잘 구분되지 않는 치주인대(치조백선의 비후 및 치주인대공간 크기의 감소 등이 영상학적 소견으로 확인된다.
-
Stage 1
증상이 없고, 감염의 증거는 없으나, 노출 및 괴사된 골 또는 골까지 탐침되는 누공이 있다. ‘Stage 0’과 유사한 영상소견이 치조골 내에 국한되어 보일 수 있다.
-
Stage 2
감염의 증거를 동반한 노출 및 괴사된 골 또는 골까지 탐침되는 누공이 있다. 이 단계에서는 통상적으로 환자에게 증상이 있다. 또한 ‘Stage 0’과 유사한 영상소견이 치조골 내에 국한되어 보일 수 있다.
-
Stage 3
감염의 증거를 동반한 노출 및 괴사된 골 또는 골까지 탐침되는 누공이 있으며, 다음 중 하나 이상의 증상을 동반한다. 괴사골이 치조골보다 확장되어 노출된 경우(예: 아래턱뼈 하연, 위턱굴, 관골 등), 병적 골절, 구외(extra-oral)누공, 구강 위턱굴 또는 비강과의 개통, 아래턱뼈 하연 또는 위턱굴까지 확대된 골용해(osteolysis)가 있다.
3. 약물 관련 악골 괴사증의 역학(Epidemiology of MRONJ)_유병률 및 발생률
-
암환자
13,857명의 환자를 대상으로 한 체계적 검토 및 메타 분석에 따르면 졸레드로네이트(zoledronate)를 투여받은 암환자에서 ONJ 유병률은 1년 후 0.4~1.6%, 2년후 0.8~2.1%, 3년후 1.0~2.3%, 데노수맙(denosumab)을 투여 받은 암환자에서 유병률은 1년후 0.5~2.1%, 2년후 1.1~3.0%, 3년후 1.3~3.2%로 나타났다.3 International Task Force on Osteonecrosis of the Jaw에서는 졸레드로네이트를 포함한 정맥주사로 치료한 환자의 발생률이 100,000명당 0~12,222명이나, 데노수맙으로 치료 한 암환자에서 100,000명당 0~2,316명으로 나타났다.4
-
골다공증 약물 복용자
골다공증 환자에서 ONJ 유병률은 호주, 캐나다, 독일, 미국, 스웨덴에서 0.001~0.01% 나타난다. 비스포스포네이트 경구 복용자의 유병률은 0.001%미만이지만, 0~0.04%까지 보고되고 있다.4,5,6,7,8 골다공증 치료를 위해 경구 비스포스포네이트를 복용하는 환자에서 발생률은 100,000명당 0~90명이며, 데노수맙을 투여 받은 환자에서 발생률은 100,000명당 0~30.2명으로 나타났다.4
-
혈관형성 억제제 사용자
베바시주맙을 투여 받는 진행성 유방암 환자에서 ONJ 유병률이 0.3~0.4%인 반면, 베바시주맙과 비스포스포네이트 병용 용법에서의 유병률은 0.9~2.4%로 나타났다.9
-
기타 약물 사용자
티로신 키나제 억제제 tyrosine kinase inhibitors (sunitinib, sorafenib, pazopanib, axitinib),10,11,12 imatinib13, regorafenib14, cabozantanib15사용 시 ONJ를 유발할 가능성이 있는 것으로 보고되었다.
단일 클론항체 Monoclonal antibodies (rituximab, adalimumab, infliximab, , romosozumab)도 ONJ를 유발할 가능성이 있다고 보고되었다.(rituximab 2건16,17 adalimumab, infliximab 4건18, romosozumab 2건19)
mTOR억제제 mTOR inhibitors(everolimus, temsirolimus), 면역억제제 immunosuppressants(methotrexate, corticosteroids)도 ONJ를 유발할 수 있으나, 위 약물 모두 극히 드물게 나타나므로 주의가 필요하다.10,11
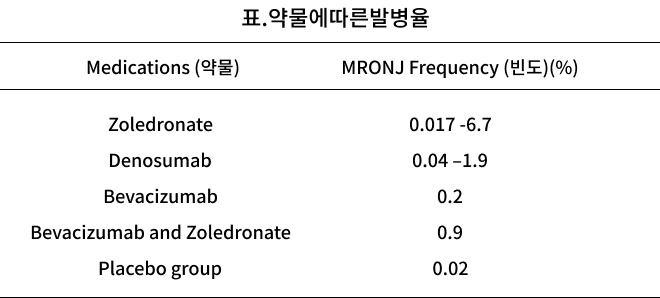
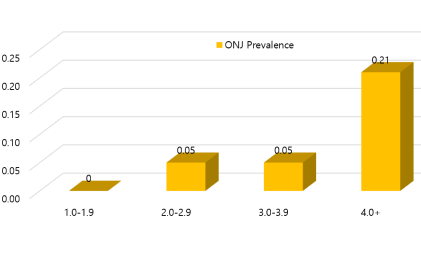
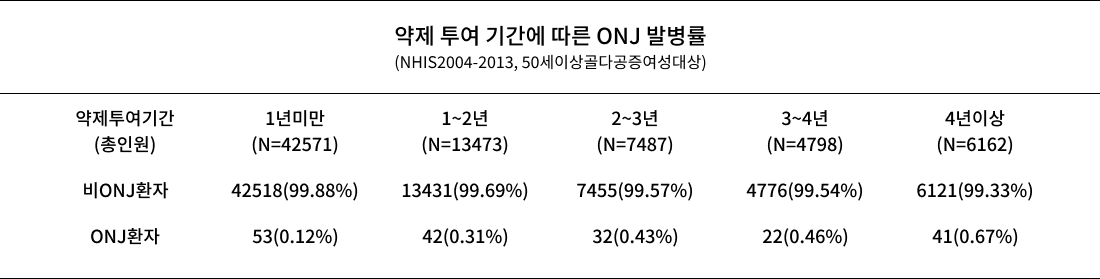
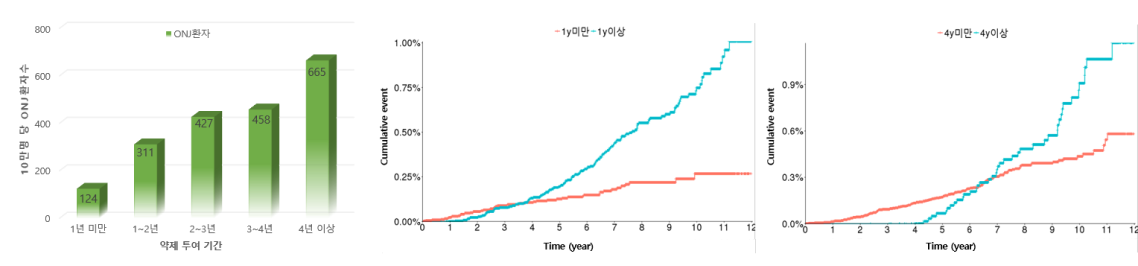
- 국내 보건의료 빅데이터를 이용한 약제 투여기간에 따른 악골괴사증 발병률(국민건강보험자료, 2004-2013코호트 이용) 발병률(국민건강보험자료, 2004-2013코호트 이용)
References
- 1. Ruggiero, Salvatore L., et al. "American Association of Oral and Maxillofacial Surgeons position paper on medication-related osteonecrosis of the jaw—2014 update." Journal of oral and maxillofacial surgery 72.10 (2014): 1938-1956.
- 2. Cosman, Felicia, et al. "Romosozumab treatment in postmenopausal women with osteoporosis." New England Journal of Medicine 375.16 (2016): 1532-1543.
- 3. Limones, Alvaro, et al. "Medication-related osteonecrosis of the jaws (MRONJ) in cancer patients treated with denosumab VS. zoledronic acid: a systematic review and meta-analysis." Medicina oral, patologia oral y cirugia bucal 25.3 (2020): e326.
- 4. Khan, Aliya A., et al. "Diagnosis and management of osteonecrosis of the jaw: a systematic review and international consensus." Journal of Bone and Mineral Research 30.1 (2015): 3-23.
- 5. Khan, Aliya A., et al. "Case-based review of osteonecrosis of the jaw (ONJ) and application of the international recommendations for management from the international task force on ONJ." Journal of clinical densitometry 20.1 (2017): 8-24.
- 6. Ulmner, Mattias, Fredrik Jarnbring, and Ove Törring. "Osteonecrosis of the jaw in Sweden associated with the oral use of bisphosphonate." Journal of oral and maxillofacial surgery 72.1 (2014): 76-82.
- 7. Svejda, B., et al. "Position paper on medication-related osteonecrosis of the jaw (MRONJ)." Wiener medizinische Wochenschrift (1946) 166.1-2 (2016): 68-74.
- 8. Mavrokokki, Tony, et al. "Nature and frequency of bisphosphonate-associated osteonecrosis of the jaws in Australia." Journal of Oral and Maxillofacial Surgery 65.3 (2007): 415-423.
- 9. Guarneri, Valentina, et al. "Bevacizumab and osteonecrosis of the jaw: incidence and association with bisphosphonate therapy in three large prospective trials in advanced breast cancer." Breast cancer research and treatment 122.1 (2010): 181-188.
- 10. King, Rebecca, Nikki Tanna, and Vinod Patel. "Medication-related osteonecrosis of the jaw unrelated to bisphosphonates and denosumab—a review." Oral surgery, oral medicine, oral pathology and oral radiology 127.4 (2019): 289-299.
- 11. Nicolatou-Galitis, Ourania, et al. "Osteonecrosis Of The Jaw Related To Non-Antiresorptive Medications/Therapies: A Systematic Review." Annual Meeting 2018 Supportive Care in Cancer MASCC/ISOO ANNUAL MEETING ON SUPPORTIVE CARE IN CANCER. Vol. 26. No. Supplement 2. Springer, 2018.
- 12. Zhang, Xiaoyan, et al. "Osteonecrosis of the jaw in the United States Food and Drug Administration's adverse event reporting system (FAERS)." Journal of Bone and Mineral Research 31.2 (2016): 336-340.
- 13. Viviano, Massimo, Marco Rossi, and Serena Cocca. "A rare case of osteonecrosis of the jaw related to imatinib." Journal of the Korean Association of Oral and Maxillofacial Surgeons 43.2 (2017): 120-124.
- 14. Antonuzzo, Lorenzo, et al. "Regorafenib also can cause osteonecrosis of the jaw." JNCI: Journal of the National Cancer Institute 108.4 (2016).
- 15. Marino, Roberto, et al. "Osteonecrosis of the jaw in a patient receiving cabozantinib." Australian dental journal 60.4 (2015): 528-531.
- 16. Allegra, Alessandro, et al. "Association of osteonecrosis of the jaws and POEMS syndrome in a patient assuming rituximab." Journal of Cranio-Maxillofacial Surgery 42.4 (2014): 279-282.
- 17. Keribin, Pierre, et al. "Osteonecrosis of the jaw in a patient presenting with post-transplantation lymphoproliferative disorder treated with rituximab: a case report." Journal of Oral and Maxillofacial Surgery 75.12 (2017): 2599-2605.
- 18. Sacco, R., et al. "Osteonecrosis and osteomyelitis of the jaw associated with tumour necrosis factor-alpha (TNF-α) inhibitors: a systematic review." British Journal of Oral and Maxillofacial Surgery 58.1 (2020): 25-33.
- 19. Cosman, Felicia, et al. "Romosozumab treatment in postmenopausal women with osteoporosis." New England Journal of Medicine 375.16 (2016): 1532-1543.
1. 치료(Treatment)
-
보존적 치료(Conservative Management)
보존적 치료로는 구강위생 관리, 치아 및 치주조직의 질환 제거, 0.12% 클로르헥시딘 (chlorhexidine)과 같은 국소 항균세정액의 사용, 전신적 항생제(페니실린, 퀴놀론(quinolones), 메트로니다졸(metronidazole), 클린다마이신(clindamycin), 독시클라인(doxycycline), 에드로마이신(erythromycin)등) 사용 등이 있다. 항생제 사용을 포함한 보존적 관리는 진행성 감염에서 직접적 효과가 미약하여 보존적 치료를 통해 병소를 완전 제거할 수는 없으나, 증상을 완화시키는 것으로 보고된다.1,2
-
수술적 치료
괴사골 제거부터 광범위한 악골 절제 및 재건 등이 해당되고, 이러한 수술적 치료를 통해 감염된 골을 제거하여야 완치되는 것으로 알려져 있다.3 괴사골이 잔존되어 있을 경우 골의 치유를 방해하고 지속적으로 연조직을 자극할 수 있어, 괴사골 또는 부골의 제거 및 적절한 치료가 되도록 해야 한다.2,4
수술 전 장기간(23-54일) 항생제 치료를 한 경우 단기(1-8일) 항생제 치료보다 수술의 성공률을 향상시켰다. 5 rhBMP-2 (Recombinant Human one Morphogenic Protein-2)6,7, L-PRF (Leukocyte-rich and Platelet-Rich Fibrin)6,8, PDGF (Platelet-Derived Growth Factor)9, PRP (Platelet Rich Plasma)9,10를 수술적 치료에 동반하면 치유가 촉진됨이 보고되었다. 추가적인 술식으로 Intraoperative fluorescence guidance11 및 Laser-assisted surgical debridement10가 보고된 바가 있다.
2. 약물 휴지기(Drug Holiday)
ONJ의 발생 원인 중 하나인 비스포스포네이트의 장기복용은 골재형성을 과도하게 억제하므로 ONJ가 발생되었거나 장기적으로 골흡수제제를 복용하고 있는 경우 drug holiday를 갖도록 권고하고 있다.12 대체 처방으로 칼시토닌(calcitonin) 또는 선택적 여성호르몬 수용체 조절체(Selective Estrogen Receptor Modulators, SERMs) 투약을 고려할 수 있다.
그러나 비스포스포네이트 drug holiday 동안 사용되는 대체약물에 대한 유효성, 지속성 그리고 ONJ에 대한 영향에 대해 대규모 조사가 이루어지지는 않은 문제점이 있다.13 또한 무조건적으로 drug holiday를 적용하지는 못하며, 골절 위험도가 높은 골다공증 환자 또는 ONJ가 발생하였음에도 악성종양으로 골전이에 의한 통증이 심하거나 고칼슘혈증이 심한 경우에는 비스포스포네이트 치료를 유지해야 하는 경우가 있다.
비스포스포네이트는 복용 후 골에 수년간 잔존되지만, 극히 낮은 ONJ 발생률을 보이므로 drug holiday를 시행해야 한다는 명확한 근거가 없다는 의견14 이 있으며, 발치 전 단기간 약물 중단은 ONJ 발생에 영향을 주지 않는다는 연구15 도 있다.
미국 치과의사협회(ADA)에서 비스포스포네이트(2년 이하 투약) 또는 데노수맙(denosumab)의 누적 복용량이 낮은 환자의 경우, 침습적 치과치료 중에도 항흡수치료 (antiresorptive therapy)를 지속할 수 있다고 제안하였다. 또한 비스포스포네이트 4년 이상 경구 투여한 경우 발생률이 급격히 증가하기 때문에, 다음의 경우에는 전신적 상태를 고려하여 수술 2달전 drug holiday를 검토해 볼 것을 권장하며, 골치유가 될 때까지 비스포스포네이트 복용 중단을 권고하고 있다.2
- 경구 비스포스포테이트 4년 미만 복용, 코르티코스테로이드나 혈관형성억제제를 병행하여 복용하는 자
- 병행하는 의학적 치료와 상관없이 경구 비스포스포네이트를 4년 이상 지속적으로 복용한 자
International Task Force on ONJ에서는 다음과 같은 환자들에게 상처가 치유될 때까지는 약물 휴지기를 가질 것을 권고하고 있다.
- 4년 이상으로 누적 비스포스포네이트 노출이 더 많은 자
- 류마티스 관절염, 현재 또는 이전에 글루코코르티코이드에 노출된 자
- 당뇨병, 흡연과 같은 위험 요인을 동반하는 자
3. Recombinant human PTH 1-34(Teriparatide)
테리파라티드(Teriparatide)는 골형성을 촉진 및 증가시키는 골다공증 치료제로서 골절감소에 효과적이다.16,17 여러 연구에서 테리파라티드로 ONJ 치료 시 효과를 보았으며2,18-21, 괴사골 제거와 약물투여를 병행할 경우 증상이 개선된다고 보고되었다.21
그러나 한 동물실험에서 테리파라티드 사용으로 골육종 (Osteosarcoma)의 발생이 보고되어, 악성종양으로 방사선치료를 받은 적이 있거나 골전이가 진행되는 경우에는 사용이 제한된다. 일본의 다기관 연구에서는 테리파라티드의 사용으로 환자의 75.9%는 효과를 보았으며, 65.6%는 완치되었다고 보고하였다. 경구제제 및 정주제제를 복용한 환자에서는 각각 83.3%, 40%의 치료효과를 보였다.22
테리파라티드를 일간 또는 주간으로 적용한(Daily ∙ Weekly injection) 효과를 비교한 연구에서는 6개월간 매일 주사한 군에서 유의하게 MRONJ 단계가 개선되었다.21 기존 치료법과 비교한 연구에서는 보존적 치료(기존방법)를 통해 60%의 치료효과를 보였으나, 6개월간 매일 20μg를 주사한군에서는 완치를 포함하여 모든 환자에서 치료효과가 나타났다.21 테리파라티드 치료 시 골밀도 증가와 더불어 ONJ 치료를 촉진하는 효과를 얻을 수 있다고 보고된다.19
항흡수제제로 치료하는 모든 환자 중 발생하지 않은 ONJ로 인해 테리파라티드로 전환해야 한다는 근거는 없다. 하지만 ONJ가 발생된 골다공증 환자에서는 테리파라티드로 전환하여 치료할 가치 있다.14
4. 약제 투여 전 사전 치과검진의 중요성
약제 투여 전 치과검진을 받은 환자에서 ONJ 발병률이 유의하게 감소하였다. 비스포스포네이트 계열 약물을 투여 받은 966명을 대상으로 한 연구에서 예방적 치과검진의 적용 전후로 ONJ 발병률은 3.2%에서 1.3%로 감소하였다.23 또 다른 연구에서는 ONJ발병률이 8.6~10.8%이었으나, 예방적 치과검진을 시행한 후에는 약0%로 감소하였다.24 한 분석을 통해 2332명의 악성종양 환자 중 예방적 치과검진을 한 경우 ONJ 발병률이 77.3% 감소한다는 것이 밝혀졌다.25 위험이 있는 환자는 예방적 치과검진을 시행하는 것이 ONJ발병률을 줄이는데 효과적인 전략이 될 수 있다.
대부분 치과 수술 이후에 ONJ가 발생하므로, 항흡수제제 치료를 계획할 때에는 투여 전 치과검진을 통해 예후가 불량한 치아를 미리 제거하거나, 필요한 치과적 수술을 진행하고 적절한 골 또는 점막치유(약14-21일)가 될 때까지 치료를 연기하는 것이 권고된다.2 예방적 치과검진, 우식 조절, 보존적 수복 치료 등은 기능적으로 건전한 치아를 유지하는데 중요하며, 의치를 사용하는 경우 점막외상부위가 있는지 주의 깊게 점검하고 환자가 구강위생을 잘 유지할 수 있도록 교육해야 한다.
5. ONJ 진단과 예후 예측을 위한 바이오 마커(biomarker)의 유효성
2007년 Marx등이 위험도 예측을 위해C-terminal telopeptide (CTX, 골흡수에 특이적인 표지자. 혈액을 통해 검사 가능) level을 ONJ 진단 목적으로 제시하였다.2 150pg/ml 이하의 혈청 CTX 수치를 보이는 환자는 ONJ 유발 가능성이 높으며 특별한 주의를 요한다고 주장하였으나, 최근 발표된 많은 연구 결과에 의하면 이는 효용성이 떨어져 CTX level과 같은 골교체표지자의 사용을 권하지 않고 있다.26 TRACP 5b 등의 골표지자를 이용하여 위험도를 예측할 수 있는 임상 연구가 활발하게 이뤄지고 있으나 바이오마커의 유효성 검증에 대한 추가적인 연구는 더 필요한 실정이다.
References
- 1. Ji, Xiaojie, et al. "Antibiotic effects on bacterial profile in osteonecrosis of the jaw." Oral diseases 18.1 (2012): 85-95.
- 2. Ruggiero, Salvatore L., et al. "American Association of Oral and Maxillofacial Surgeons position paper on medication-related osteonecrosis of the jaw—2014 update." Journal of oral and maxillofacial surgery 72.10 (2014): 1938-1956.
- 3. Favia, G., et al. "Medication‐related osteonecrosis of the jaw: Surgical or non‐surgical treatment?" Oral diseases 24.1-2 (2018): 238-242.
- 4. Rugani, Petra, et al. "Stage-related treatment concept of medication-related osteonecrosis of the jaw—a case series." Clinical oral investigations 19.6 (2015): 1329-1338.
- 5. Hoefert, Sebastian., et al. "Relevance of a prolonged preoperative antibiotic regime in the treatment of bisphosphonate-related osteonecrosis of the jaw." Journal of Oral and Maxillofacial Surgery 69.2 (2011): 362-380.
- 6. Park, Jung-Hyun., et al. "Does the addition of bone morphogenetic protein 2 to platelet-rich fibrin improve healing after treatment for medication-related osteonecrosis of the jaw?" Journal of oral and maxillofacial surgery 75.6 (2017): 1176-1184.
- 7. Mikai, Akihiro, et al. "BMP-2/β-TCP Local Delivery for Bone Regeneration in MRONJ-Like Mouse Model." International journal of molecular sciences 21.19 (2020): 7028.
- 8. Cano-Durán, Jorge A., et al. "The role of Leucocyte-rich and platelet-rich fibrin (L-PRF) in the treatment of the medication-related osteonecrosis of the jaws (MRONJ)." Journal of clinical and experimental dentistry 9.8 (2017): e1051.
- 9. Longo, F., et al. "Platelet rich plasma in the treatment of bisphosphonate-related osteonecrosis of the jaw: personal experience and review of the literature." International journal of dentistry 2014 (2014).
- 10. Martins, Marco Antonio T., et al. "Association of laser phototherapy with PRP improves healing of bisphosphonate-related osteonecrosis of the jaws in cancer patients: a preliminary study." Oral oncology 48.1 (2012): 79-84.
- 11. Pautke, Christoph, et al. "Fluorescence-guided bone resection in bisphosphonate-related osteonecrosis of the jaws: first clinical results of a prospective pilot study." Journal of Oral and Maxillofacial Surgery 69.1 (2011): 84-91.
- 12. Watts, Nelson B., and Dima L. Diab. "Long-term use of bisphosphonates in osteoporosis." The Journal of Clinical Endocrinology & Metabolism 95.4 (2010): 1555-1565.
- 13. Kim, Kyoung Min, et al. "Medication related osteonecrosis of the jaw: 2015 position statement of the Korean Society for Bone and Mineral Research and the Korean Association of Oral and Maxillofacial Surgeons." Journal of bone metabolism 22.4 (2015): 151.
- 14. Khan, Aliya A., et al. "Diagnosis and management of osteonecrosis of the jaw: a systematic review and international consensus." Journal of Bone and Mineral Research 30.1 (2015): 3-23.
- 15. Hasegawa, T., et al. "A multicenter retrospective study of the risk factors associated with medication-related osteonecrosis of the jaw after tooth extraction in patients receiving oral bisphosphonate therapy: can primary wound closure and a drug holiday really prevent MRONJ?" Osteoporosis International 28.8 (2017): 2465-2473.
- 16. Blick, Stephanie K A et al. “Teriparatide: a review of its use in osteoporosis.” Drugs vol. 68,18 (2008): 2709-37.
- 17. Rubin, Mishaela R, et al. “The anabolic effects of parathyroid hormone therapy.” Clinics in geriatric medicine vol. 19,2 (2003): 415-32.
- 18. Subramanian, Gayathri, Harold V, et al. "A model for the pathogenesis of bisphosphonate-associated osteonecrosis of the jaw and teriparatide's potential role in its resolution." Oral Surgery, Oral Medicine, Oral Pathology, Oral Radiology, and Endodontology 112.6 (2011): 744-753.
- 19. Kwon, Yong-Dae, et al. "Role of teriparatide in medication-related osteonecrosis of the jaws (MRONJ)." Dentistry journal 4.4 (2016): 41.
- 20. Kim, Jun-Young, et al. "Treatment of medication-related osteonecrosis of the jaw around the dental implant with a once-weekly teriparatide: A case report and literature review." Journal of Oral Implantology 45.5 (2019): 403-407.
- 21. Ohbayashi, Y., et al. "A comparative effectiveness pilot study of teriparatide for medication-related osteonecrosis of the jaw : daily versus weekly administration." Osteoporosis International 31.3 (2020): 577-585.
- 22. Morishita, Kota, et al. "Treatment outcomes of adjunctive teriparatide therapy for medication-related osteonecrosis of the jaw (MRONJ): A multicenter retrospective analysis in Japan." Journal of Orthopaedic Science 25.6 (2020): 1079-1083.
- 23. Ripamonti, C I et al. “Decreased occurrence of osteonecrosis of the jaw after implementation of dental preventive measures in solid tumour patients with bone metastases treated with bisphosphonates. The experience of the National Cancer Institute of Milan.” Annals of oncology : official journal of the European Society for Medical Oncology vol. 20,1 (2009): 137-45.
- 24. Bramati, Annalisa, et al. "Prospective, mono-institutional study of the impact of a systematic prevention program on incidence and outcome of osteonecrosis of the jaw in patients treated with bisphosphonates for bone metastases." Journal of bone and mineral metabolism 33.1 (2015): 119-124.
- 25. Karna, Harry, et al. "Risk-reductive dental strategies for medication related osteonecrosis of the jaw among cancer patients: a systematic review with meta-analyses." Oral oncology 85 (2018): 15-23.
- 26. Awad, Mohamed E., et al. "Serum C-terminal cross-linking telopeptide level as a predictive biomarker of osteonecrosis after dentoalveolar surgery in patients receiving bisphosphonate therapy: Systematic review and meta-analysis." The Journal of the American Dental Association 150.8 (2019): 664-675.
